化妆品中非那西丁的检验方法
Determination of Phenacetin in Cosmetics
1 范围
本方法规定了液相色谱-串联质谱法测定化妆品中非那西丁的含量。
本方法适用于膏霜乳类、液体类、凝胶类、粉类等化妆品中非那西丁的定性与定量。
2 方法提要
样品以乙腈为溶剂提取,采用高效液相色谱仪分离,质谱检测器检测,根据保留时间和特征离子对的相对丰度比定性、定量离子对峰面积定量,以标准曲线法计算含量。
本方法取样量为0.5 g时,检出浓度为0.012 mg/kg,最低定量浓度为0.04 mg/kg。
3 试剂和材料
除另有规定外,本方法所用试剂均为分析纯或以上规格,水为GB/T 6682规定的一级水。
3.1 甲醇,色谱纯。
3.2 乙腈,色谱纯。
3.3 氯化钠。
3.4 50%乙腈:取乙腈、水等体积混合,摇匀。
3.5 饱和氯化钠溶液:称取40 g氯化钠(3.3),置于250 mL磨口锥形瓶中,加入100 mL水,超声15 min,即得。
3.6 标准品:非那西丁(英文名称:Phenacetin,分子式:C10H13NO2,CAS:62-44-2),纯度≥98%。
3.7 标准储备溶液:精密称取非那西丁标准品10 mg(精确到0.00001 g)于10 mL容量瓶中,加入甲醇(3.1)溶解并定容,配制成质量浓度为1 mg/mL的标准溶液备用,转入棕色储液瓶中,4 ℃避光保存,有效期3个月。
3.8 标准中间液:精密量取适量标准储备溶液(3.7),用甲醇(3.1)稀释成质量浓度为10 mg/L的标准中间液。
4 仪器和设备
4.1 高效液相色谱-三重四极杆质谱联用仪。
4.2 分析天平:感量0.0001 g和0.00001 g。
4.3 超声波清洗器(≥250 W)。
4.4 涡旋混合仪。
4.5 高速离心机。
5 分析步骤
5.1 空白基质提取液
称取空白试样0.5 g(精确到0.0001 g),置于15 mL具塞比色管中,自“加入饱和氯化钠溶液2 mL”起与样品同法处理(5.4),作为空白基质提取液。该基质提取液进入质谱后,在非那西丁的特征离子峰保留时间处未出峰且未检出其特征离子对,则确认为空白基质提取液,可用于下一步实验。空白样品的性状应与待测化妆品尽量基本一致。
5.2 基质标准中间液
精密量取非那西丁标准中间液(3.8)0.1 mL,置于10 mL容量瓶中,用空白基质提取液(5.1)稀释至刻度,摇匀,制成非那西丁浓度为100 μg/L的基质标准中间液。基质标准中间液现用现配。
5.3 基质标准系列溶液的制备
精密量取基质标准中间液(5.2)0.1、0.2、0.5、1、2、5 mL,用空白基质提取液(5.1)配制浓度为1.0、2.0、5.0、10、20、50 μg/L基质标准系列溶液。基质标准系列溶液现用现配。
5.4 样品处理
膏霜乳类、液体类、凝胶类:称取样品0.5 g(精确到0.0001 g),置于15 mL离心管中,加入饱和氯化钠溶液(3.5)2 mL,涡旋30 s,分散均匀,准确加入乙腈(3.2)10 mL,涡旋30 s,超声提取10 min,静置至室温,以8000 r/min转速离心5 min。准确吸取上清液5 mL,加50%乙腈(3.4)定容至10 mL,混匀,经0.22 μm滤膜过滤后,滤液作为供试品溶液备用(供试品溶液可根据实际浓度进行适当稀释)。
粉类:称取样品0.5 g(精确到0.0001 g),置于15 mL离心管中,准确加入乙腈(3.2)10 mL,涡旋30 s,超声提取10 min,静置至室温,以8000 r/min转速离心5 min。准确吸取上清液5 mL,加50%乙腈(3.4)定容至10 mL,混匀,经0.22 μm滤膜过滤后,滤液作为供试品溶液备用(供试品溶液可根据实际浓度进行适当稀释)。
5.5 参考液相色谱-三重四极杆质谱联用条件
色谱条件
色谱柱:C18色谱柱(2.1 mm×100 mm,2.7 μm),或等效色谱柱;
柱温:30 ℃;
进样体积:2 μL;
流动相A:水,流动相B:乙腈;
流速:0.3 mL/min。
表1 梯度洗脱程序
时间(min) | 流动相A(%) | 流动相B(%) |
0.0 | 90 | 10 |
2.0 | 90 | 10 |
5.0 | 25 | 75 |
5.1 | 10 | 90 |
7.0 | 10 | 90 |
7.1 | 90 | 10 |
9.0 | 90 | 10 |
质谱条件
离子源:电喷雾离子源(ESI源);
监测模式:正离子多反应监测模式(MRM),监测离子对及相关参数设定见表2。
表2 非那西丁的监测离子对及相关参数设定
00001组分名称 | 00002母离子 00003(m/z) | 00004子离子 00005(m/z) | 00006CE 00007(V) |
00008非那西丁 | 00009180.1 | 00010110.2* | 0001126 |
00012138.1 | 0001314 |
*为推荐的定量离子。
注:当采用不同质谱仪器时,仪器参数可能存在差异,测定前应将质谱参数优化到最佳。
5.6 定性判定
取供试品溶液(5.4)与标准溶液在相同分析条件下测定,样品中如呈现定量离子对和定性离子对的色谱峰,非那西丁的特征离子峰保留时间与标准溶液对应的保留时间偏差小于±2.5%,且选择的监测离子对的相对丰度比与相当浓度的标准溶液的监测离子对的相对丰度比的最大偏差不超过表3的规定,则可以判定样品中存在非那西丁。
表3 定性确证时相对离子丰度比的最大允许偏差
相对离子丰度(k) | k>50% | 50%≥k>20% | 20%≥k>10% | k≤10% |
允许的最大偏差 | ±20% | ±25% | ±30% | ±50% |
5.7 定量测定
在“5.5”项液相色谱-三重四极杆质谱联用条件下,取基质标准系列溶液(5.3)依次测定,以非那西丁的系列浓度为横坐标,其定量离子对色谱峰面积为纵坐标,进行线性回归,绘制基质标准曲线,其线性相关系数应大于0.99。
取“5.4”项下处理得到的待测溶液进样,将非那西丁定量离子对色谱峰面积代入基质标准曲线,计算非那西丁的质量分数,按“6”项下公式,计算样品中非那西丁的含量。
6 分析结果的表述
6.1 计算
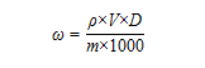
式中:ω—样品中非那西丁的质量分数,mg/kg;
ρ—供试品溶液中非那西丁的质量浓度,μg/L;
V—样品定容体积,mL;
m—样品取样量,g;
D—稀释倍数(如未稀释则为1)。
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的15%。
6.2 回收率和精密度
多家实验室验证回收率为82.6%~115.8%,相对标准偏差小于6.4%。
7 图谱
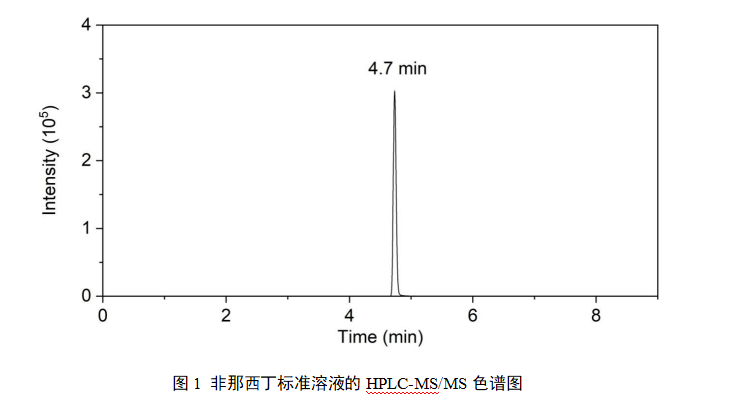
图1 非那西丁标准溶液的HPLC-MS/MS色谱图
《化妆品安全技术规范》5项标准制修订项目汇总表
序号 | 项目名称 | 类型 | 建议纳入《化妆品安全技术规范》的章节 | 同时废止的《化妆品安全技术规范》中原章节内容 |
1 | 新增检验方法 | 第四章 理化检验方法 8 其他原料检验方法 8.4 化妆品中壬二酸及其盐类的检验方法 | - | |
2 | 第四章 理化检验方法 2 禁用组分检验方法 2.39 化妆品中非那西丁的检验方法 | - | ||
3 | 第四章 理化检验方法 3 限用组分检验方法 3.14 化妆品中羟基癸酸的检验方法 | - | ||
4 | 修订后替换原检验方法 | 第四章 理化检验方法 2 禁用组分检验方法 2.27 化妆品中石棉的检验方法 | 第四章 理化检验方法 2 禁用组分检验方法 2.27 石棉 | |
5 | 第四章 理化检验方法 3 限用组分检验方法 3.1 化妆品中葡糖醛酸等14种原料的检验方法 | 第四章 理化检验方法 3 限用组分检验方法 3.1 α-羟基酸(国家药品监督管理局2019年第12号通告) |


