化妆品新原料定义:
在我国境内首次使用于化妆品天然或者人工原料为化妆品新原料--《化妆品监督管理条例》(自2021年1月1日起实施)。
除外情况:
1.收录于《已使用化妆品原料目录》 (2021年版)的原料
2.包含于已使用类别原料中的具体原料(如胶原,某某植物提取物等)3.《化妆品安全技术规范》 已规定为禁用组分的原料(如人的细胞、组织 或人源产品等)
4. 实际功能超出化妆品定义范畴的原料(如“激活细胞,再生细胞,促愈 合作用 ”等具有医疗作用的原料
化妆品原料 | 已知原料 | 准用原料 | 防腐剂(48种) |
防晒剂(26种) | |||
染发剂(73) | |||
着色剂(156种) | |||
限用原料(44种) | |||
禁用原料(1284种+109种) | |||
已使用化妆品原料(2021版)(8972种-72种) | |||
新原料 | 高风险(防腐,防晒,着色,染发,祛斑美白) | 注册 | |
低风险 | 备案 |
化妆品新原料到已知原料要求:三年监测期, 未发生安全问题可纳入已使用原料目录
化妆品新原料申报流程
化妆品新原料注册人/备案人
化妆品新原料注册人、 备案人在申报新原料注册或进行新原料备案前 , 应当通过信息服务平台 ,填报以下信息 ,进行用户信息登记:
(一) 化妆品新原料注册人、 备案人信息;
(二)化妆品新原料注册人、 备案人安全风险监测和评价体系概述;
(三)化妆品新原料注册人、 备案人为境外的 ,应当由境内责任人填报信息 , 同时提交境内 责任人授权书及其公证书的原件。
|
|
国家药品监督管理局数据查询 (nmpa.gov.cn) |
化妆品新原料注册流程图:
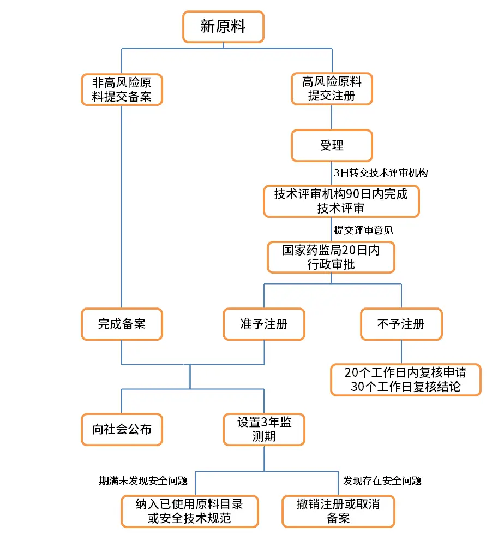
化妆品新原料监测期要求
√ 安全监测期自首次使用化妆品新原料的化妆品取得注册或者完成备案之日起算。
√ 安全监测期内 ,化妆品新原料注册人、 备案人可以使用该化妆品新原料生产化妆品。 化妆品注册人、 备案人使用 化妆品新原料生产化妆品的 ,相关化妆品申请注册、 办理备案时应当通过信息服务平台经化妆品新原料注册人、 备 案人关联确认。
√ 化妆品新原料注册人、 备案人应当在化妆品新原料安全监测每满一年前30个工作日内 ,汇总、 分析化妆品新原料使用和安全情况 ,形成年度报告报送国家药品监督管理局。
√ 发现下列情况的 ,化妆品新原料注册人、 备案人应当立即开展研究 , 并向技术审评机构报告:
(一) 其他国家(地区) 发现疑似因使用同类原料引起严重化妆品不良反应或者群体不良反应事件的;
(二)其他国家(地区) 化妆品法律、 法规、 标准对同类原料提高使用标准、 增加使用限制或者禁止使用的;
(三)其他与化妆品新原料安全有关的情况。
√ 化妆品新原料安全监测期满3年后 ,技术审评机构应当向国家药品监督管理局提出化妆品新原料是否符合安全性要求的意见。
对存在安全问题的化妆品新原料 , 由国家药品监督管理局撤销注册或者取消备案; 未发生安全问题的 , 由国家药品监督管理局纳入已使用的化妆品原料目录。
化妆品新原料申报资料要求
序号 | 项目标题 | 填报要求 | 填报形式 | 备注 |
01 信息表 | ||||
1月1日 | 注册或备案信息表 | 必须填报 | 填写 | 无法实现电子签章的(例如无法申领CA的境外注册人/备案人签章),按相关要求递交签章完整的纸质原件。 |
02 研制报告 | ||||
2月1日 | 研发背景 | 必须填报 | 上传 | 包括研发背景、研发目的、研发过程 及研发结果等 |
2月2日 | 原料基本信息 | 必须填报 | 填写/上传 | 包括原料名称、来源、组成、相对分子质量、分子式、化学结构、理化性质等信息 |
2月3日 | 原料使用信息 | 必须填报 | 填写/上传 | 包括原料在化妆品中的使用规格、使用目的、适用或使用范围、安全使用量、使用期限、注意事项、警示用语等;原料在境外使用于化妆品的状况以及批准状况 |
2月4日 | 功能依据资料 | 必须填报 | 上传 | 指能够证明原料具有与使用目的相一致的相关资料,一般包括科学文献、法规资料、实验室研究数据、人体功效性评价试验资料等 |
2月5日 | 研制相关的其他资 料 | 必须填报 | 上传 | |
03 制备工艺及质量控制标准 | ||||
3月1日 | 制备工艺简述 | 必须填报 | 上传 | 应当结合原料来源特征,对原料生产的主要工艺步骤、工艺参数等进行简要描述,并说明生产过程是否可能引入安全性风险物质及其控制措施 |
3月2日 | 稳定性试验数据 | 必须填报 | 上传 | 一般包括破坏性试验、加速试验、长期试验等实 验方法 |
3月3日 | 质量规格指标及其检验方法 | 必须填报 | 上传 | 包括原料性状及其检验方法,原料的理化性质,定性鉴别方法,原料纯度控制指标及其检验方法,原料的包装、运输和贮存要求,原料的使用目的、适用或使用范围、规格及安全的使用量、注意事项、警示用语等 |
3月4日 | 可能存在的安全性风险物质及其控制等资料 | 适用时填报 | 上传 | 如微生物、重金属、有害物质(如有害组分、有 害杂质、有害溶剂等)等控制指标 |
序号 | 项目标题 | 填报要求 | 试验周期 | 情形1 | 情形2 | 情形3 | 情形4 | 情形5 | 情形6 |
国内外首次使用+高风险功效+较高生物活性 | 国内外首次使用+非高风险功效 | 国外已使用+非高风险功效 | 国外已使用+高风险功效 | 具有食用历史 | 结构和性质稳定的聚合物 | ||||
04 安全性评价 高风险功效 :防腐、防晒、着色、染发、祛斑美白、防脱发、祛痘、抗皱、去屑、除臭 | |||||||||
4月1日 | 毒理学安全性评价综述 | 必须填报 | / | √ | √ | √ | √ | √ | √ |
4月2日 | 急性经口或急经皮毒性试验 | 适用时填报 | 25工作日 | √ | √ | √ | √ | ||
4月3日 | 皮肤和眼刺激性/腐蚀性试验 | 必须填报 | 25工作日 | √ | √ | √ | √ | √ | √ |
4月4日 | 皮肤变态反应试验 | 适用时填报 | 40工作日 | √ | √ | √ | √ | √ | |
4月5日 | 皮肤光毒性试验 | 适用时填报 | 15工作日 | ||||||
4月6日 | 皮肤光变态反应试验 | 适用时填报 | 3个月 | ||||||
4月7日 | 致突变试验 | 适用时填报 | 25工作日 | √ | √ | √ | √ | ||
4月8日 | 亚慢性经口或经皮毒性试验 | 适用时填报 | 6个月 | √ | √ | √ | |||
4月9日 | 致畸试验 | 适用时填报 | 3个月 | √ | |||||
4月10日 | 慢性毒性/致癌性结合试验 | 适用时填报 | 24个月 | √ | |||||
4月11日 | 吸入毒性试验 | 适用时填报 | 4个月 | ||||||
4月12日 | 长期人体试用安全试验 | 适用时填报 | 12个月 | √ | |||||
4月13日 | 其他毒理学试验 | 适用时填报 | / | ||||||
4月14日 | 安全性评估报告 | 必须填报 | 10工作日 | √ | √ | √ | √ | √ | √ |
05 其他资料 | |||||||||
5月1日 | 新原料技术要求 | 必须填报 | / | √ | √ | √ | √ | √ | √ |
5月2日 | 可能有助于化妆品新原料注册和备案的其他资料 | 适用时填报 | / | ||||||
化妆品新原料申报的6中情形:
1、国内外首次使用的具有防腐、防晒、着色、染发、祛斑美白、防脱发、祛痘、抗皱(物理性抗皱除外)、去屑、除臭功能以及其他国内外首次使用的具有较高生物活性的化妆品新原料:这类情形需要注册制,但目前尚未有成功案例,主要原因是申报周期长、检测费用高、未知因素多等;
2、国内外首次使用的,不具有上述功能的新原料:这类情形采用备案制,已有企业成功完成备案;
3、不具有上述功能的新原料,但能够提供充分的证据材料证明该原料在境外上市化妆品中已有三年以上安全使用历史的:这类情形也采用备案制;
4、具有防腐、防晒、着色、染发、祛斑美白、防脱发、祛痘、抗皱(物理性抗皱除外)、去屑、除臭功能,且能够提供充分的证据材料证明该原料在境外上市化妆品中已有三年以上安全使用历史的新原料:这类情形需要注册制;
5、具有安全食用历史的化妆品新原料:这类情形需要注册制,且原料所使用的部位应与食用部位一致;
6、其他情形:这类情形需要注册制,具体要求可能因具体情况而异;
申报流程和所需资料:
情形1和情形4:需要提交新原料的安全性评估报告、毒理学试验报告、人体安全性和功效性试验报告等
情形2和情形3:需要提交新原料的安全性评估报告、毒理学试验报告等
情形5:需要提交食品安全认证或其他相应资质的证明文件
化妆品检测相关报告及检验方法:
检验相关资料 | 检验报告要求 | 检验方法要求 |
1. 理化和微生物检验报告 | 自行或者委托具备相应检验能力的检验检测机构 | 原则上应当参考《化妆品安全技术规范》或者《中华人民共和国药典》等规定的检验方法。《化妆品安全技术规范》《中华人民共和国药典》未规定方法的项目,应当按照国家标准、国际通行方法或者使用自行开发的试验方法进行检验。使用自行开发试验方法的,应当同时提交该方法的适用性和可靠性相关资料。 |
2. 功能评价报告(防腐、防晒、 祛斑美白、防脱发之外) | ||
3.功能评价报告(防腐、防晒、 祛斑美白、防脱发) | 取得化妆品领域的检验检测机构资质认定(CMA)或中国合格评定国家认可委员会(CNAS)认可,或者符合国际通行的良好临床操作规范(GCP)或良好实验室操作规范(GLP)等资质认定或认可的检验机构 | |
4.毒理学试验报告 | 应当按照《化妆品安全技术规范》规定的试验方法开展。《化妆品安全技术规范》未规定方法的项目,应当按照国家标准或国际通行方法进行检验。 | |
应用的动物替代试验方法尚未收录于我国《化妆品安全技术规范》的,该项替代试验方法应当为国际权威替代方法验证机构已收录的方法, | ||
且应当同时提交该方法能准确预测该毒理学终点的证明资料。 |
如何正确理解化妆品新原料备案
备案的真实含义是新原料备案人向药品监管部门提交资料备查。化妆品新原料备案人完成备案后,国家药监局 公布新原料备案信息,仅代表该原料已完成备案资料的提交,符合形式要求,而对其资料内容的真实性、科学性、 充分性可能尚未核查。公开已完成备案的化妆品新原料相关信息不代表认可该新原料的安全性与功能性,更无所谓的“成功获得批准备案 ”的说法。
根据《条例》 《办法》规定,化妆品新原料完成备案后,药品监督管理部门将组织技术审评机构对新原料的备 案资料开展技术核查,并对化妆品新原料的使用和安全情况进行跟踪评估,发现已备案化妆品新原料的备案资料不 符合要求的,将责令限期改正。
与化妆品新原料安全性有关的备案资料不符合要求的,可以同时责令暂停新原料的销售、使用;发现化妆品新 原料不属于备案范围,或者备案时提交虚假资料等问题的,将取消化妆品新原料的备案;化妆品新原料被责令暂停 使用或者取消备案,化妆品注册人、备案人应当同时暂停或者停止生产、经营使用该新原料的化妆品。
如何判定化妆品新原料应当申请注册或进行备案
通常情况下,针对具备多种功能的新型化妆品原料而言,倘若其中某一项功能处于应当申报注册的范畴之内,那么该新原料便需要依据《规定》来开展申报注册工作,唯有在获得批准注册之后才能够投入使用。而若其同时拥有的众多功能均未处于应当申报注册的情形之中,那么不管功能的种类有多少,都只需在使用之前依照《规定》向国家药监局完成备案流程即可。
化妆品新原料的注册人以及备案人绝对不可以蓄意隐瞒新原料实际所具备的功能,也不能将本应申报注册的化妆品新原料仅仅进行备案操作后就应用于化妆品的生产制造过程。一旦这种行为被核实查证,将会依据《条例》第五十九条第三项的相关规定予以惩处。
化妆品案例相关阅读:
化妆品功效测试相关阅读: