皮肤致敏性整合测试与评估策略应用技术指南
——“3选2试验”策略
一、概述
皮肤变态反应(过敏性接触性皮炎Skin sensitization, allergic contact dermatitis),是皮肤对一种物质产生的免疫源性皮肤反应。皮肤变态反应试验是评价化妆品原料致敏性的常用方法,随着动物福利及科学技术的发展,国际上也逐步开展采用体外试验、非测试的毒性预测方法等多种毒理学评价工具组合的皮肤致敏性整合测试与评估策略,用于评价化妆品原料的潜在致敏风险。
目前科学上普遍认可皮肤过敏是以蛋白质共价结合为起始事件,经过细胞、组织器官等一系列生物学应答,最终导致过敏性接触性皮炎这一有害结局。皮肤致敏性整合测试与评估策略基于皮肤致敏有害结局路径(Adverse Outcome Pathway,AOP)以及针对其中各关键事件(Key Events,KEs)研发的系列替代毒理学试验,整合待评估原料相关数据进行证据权重分析,对化妆品原料潜在的皮肤致敏性风险进行评价。
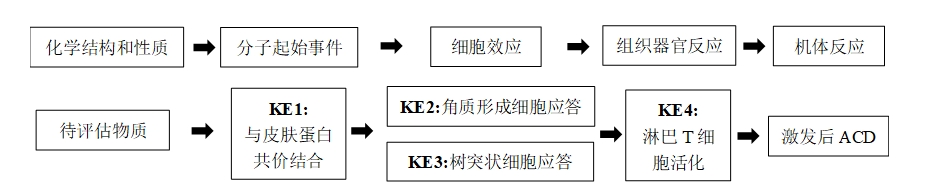
图1 皮肤致敏AOP示意图
在皮肤致敏性AOP中,关键事件KE1为分子起始事件,关键事件KE2和KE3分别为角质形成细胞免疫应答和树突状细胞免疫应答,关键事件KE4为组织器官免疫应答反应(淋巴T细胞增殖)。
二、适用范围
本应用指南适用于化妆品原料皮肤致敏性评价。采用皮肤致敏性AOP检测关键事件KE1~KE3的毒理学试验方法组成“3选2试验”策略,其适用范围应符合所选所有试验方法适用性的要求。
三、基本原则
结合化妆品原料的特点,基于皮肤致敏AOP的机制,形成固定的逐步获取和评估检测数据的顺序测试策略,根据所获得的检测结果决定是否需要开展后续检测,可对化妆品原料皮肤致敏性进行危害识别。在策略中应说明覆盖了AOP中哪些关键事件、试验方法的选择顺序、对已知不确定性的考虑(如所选试验方法局限性、阳性结果判定的阈值边界范围等)内容。
四、可用的替代方法
目前,《化妆品安全技术规范》中用于检测皮肤致敏性的替代方法包括:皮肤变态反应:局部淋巴结试验(LLNA:DA和LLNA: BrdU-ELISA),体外皮肤变态反应试验:直接多肽反应试验(DPRA)、氨基酸衍生化反应试验方法(ADRA)、人细胞系活化试验(h-CLAT)、U937细胞激活试验方法(U-SENS)和角质细胞荧光素报告基因测试LuSens方法(LuSens)。
表1 皮肤致敏性替代试验结果判定要求
关键事件 | 方法名称 | 结果判定要求 |
KE1 | 化妆品用化学原料体外皮肤变态反应:直接多肽反应试验(DPRA) | 详见附录1 |
体外皮肤变态反应 氨基酸衍生化反应试验方法(ADRA) | 需说明结果判定及不确定分析 | |
KE2 | 体外皮肤变态反应 角质细胞荧光素报告基因测试LuSens方法(LuSens) | 详见附录2 |
KE3 | 体外皮肤变态反应 人细胞系活化试验(h-CLAT) | 详见附录3 |
体外皮肤变态反应 U937细胞激活试验(U-SENS) | 需说明结果判定及不确定分析 | |
KE4 | 皮肤变态反应:局部淋巴结试验:DA(LLNA:DA) | 可得出受试物致敏能力和强度 |
皮肤变态反应:局部淋巴结试验:BrdU-ELISA(LLNA:BrdU-ELISA) |
其中局部淋巴结试验(LLNA:DA和LLNA: BrdU-ELISA)用于检测KE4,试验结果能得出受试物的致敏能力和强度,这些结果可在有限的范围内外推到人类。
DPRA和ADRA试验用于检测KE1;LuSens试验用于检测KE2;h-CLAT和U-SENS试验用于检测KE3。“3选2试验”策略应从KE1~KE3中任意选择两个关键事件,分别选择对应的一项试验方法进行检测,如两个关键事件检测结论一致且试验结果均不在阈值边界范围内,则根据一致的结论判定化妆品原料是否具有皮肤致敏性;否则开展第三个关键事件的检测,根据三个关键事件检测结论中一致的两项结论判定化妆品原料是否具有皮肤致敏性;若三个关键事件检测结论存在矛盾(一项为阳性结果、一项为阴性结果、一项结果在阈值边界范围内)或其中两项以上检测结果均在阈值边界范围内,则判定无法确定皮肤致敏性风险。
五、注意事项
“3选2试验”策略的可靠性受组成策略的试验方法的适用性和局限性、原料理化性质等多种因素综合影响,预测结果存在一定的不确定性,需在评估过程中予以说明。例如,采用h-CLAT方法时,要求受试物具有可溶性,对正辛醇-水分配系数(LogKow)>3.5的原料,易出现假阴性的结果,可采用其他检测该关键事件的试验方法组成策略或选择其他皮肤致敏性评价方法,如皮肤变态反应试验或局部淋巴结试验等。
虽然每一项试验方法具有明确的阳性结果判定阈值,但接近阈值的检测结果在组成策略时,会降低结论的可信度,通过统计试验方法验证数据可获得阳性判定的阈值边界范围(borderline range),检测结果在阈值边界范围内的可采用其他检测该关键事件的试验方法组成策略或选择其他皮肤致敏性评价方法。
本指南及附录仅以DPRA、LuSens和h-CLAT试验作为“3选2试验”策略示例,如选用尚未收录于我国《化妆品安全技术规范》的其他国际权威替代方法验证机构发布的方法时,应说明方法适用性、检测关键事件、结果判定及不确定分析(如阈值边界范围等)。
附录1
直接多肽反应试验(DPRA)
按照DPRA的要求开展检测。根据试验结果判定标准,当采用1:10半胱氨酸多肽和1:50赖氨酸多肽模型判定时,阳性结果判定值为6.38%,阈值边界范围为4.95%~8.32%;当采用1:10半胱氨酸多肽模型判定时,阳性结果判定值为13.89%,阈值边界范围为10.56%~18.47%。结果判定策略如图2。

1:10半胱氨酸多肽和1:50赖氨酸多肽模型
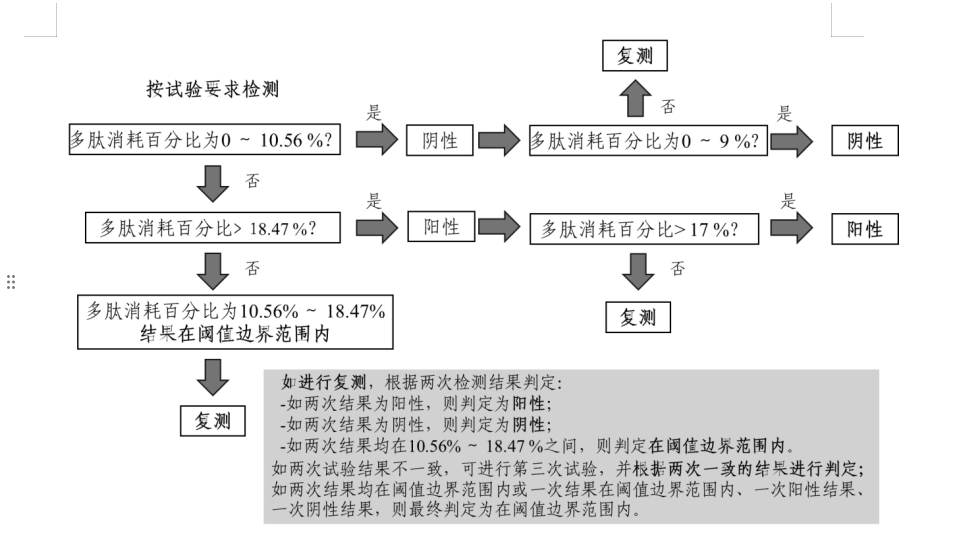
1:10半胱氨酸多肽模型
图2 DPRA策略程序示意图
附录2
角质细胞荧光素报告基因测试LuSens法
按照LuSens的要求开展检测。根据试验结果判定标准,阳性结果判定值为1.5倍,阈值边界范围为1.28~1.76倍。结果判定策略如图3。
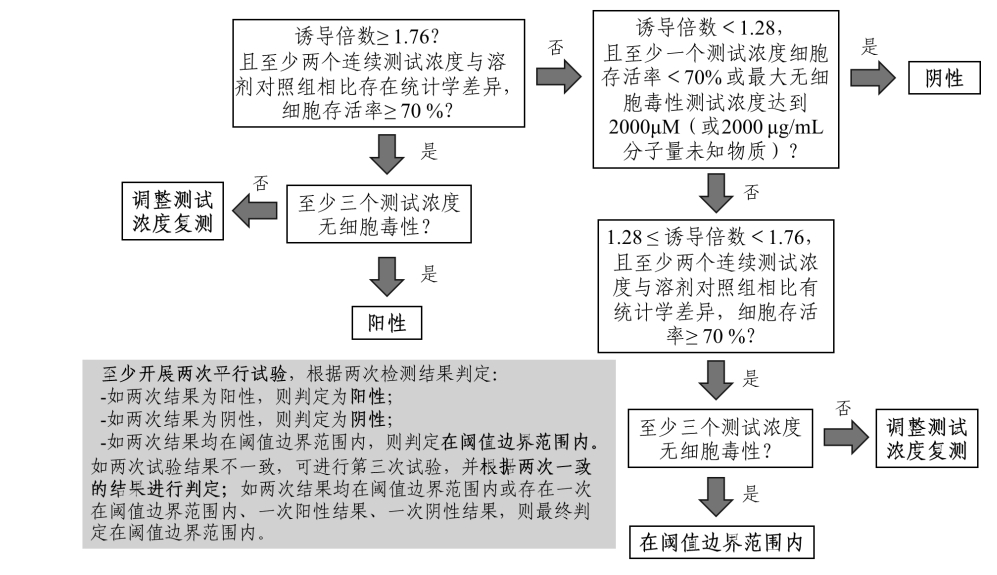
图3 LuSens策略程序示意图
附录3
人细胞系活化试验(h-CLAT)
按照h-CLAT的要求开展检测。根据试验结果判定标准,阳性结果判定值CD86诱导值为150%,阈值边界范围为122%~184%,CD54诱导值为200%,阈值边界范围为157%~255%。结果判定策略如图4。
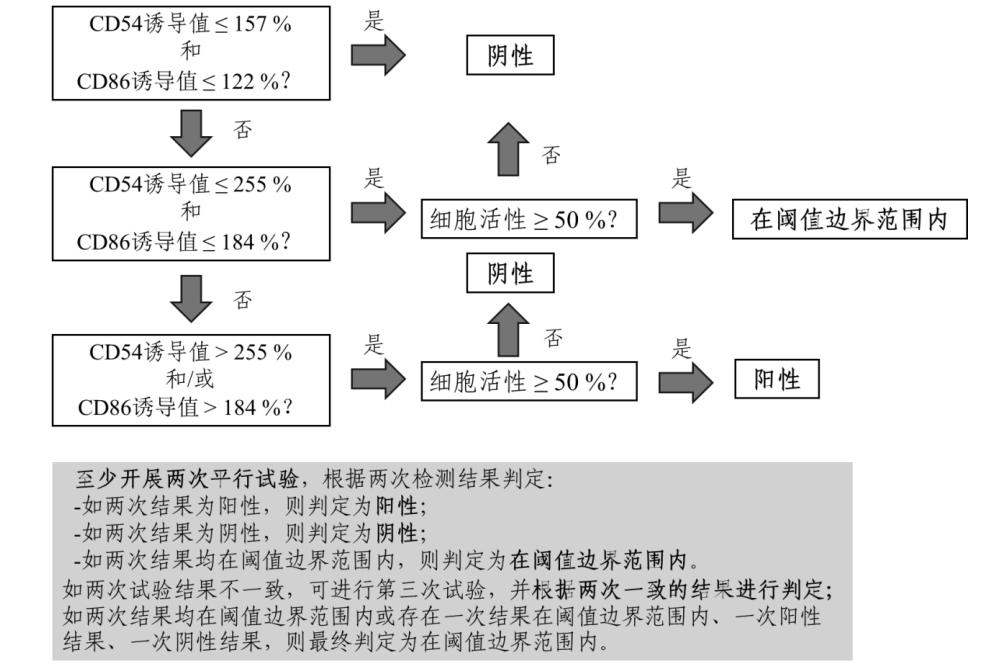
图4 h-CLAT策略程序示意图
附录4
化妆品原料“3选2试验”策略应用示例
注:实例所用数据非真实数据,仅为展示策略步骤
1.待评估物质信息
无色透明液体,LogKow<3.5。其他信息略。
2.“3选2”试验策略示例
步骤一:开展DPRA试验,采用1:10半胱氨酸多肽和1:50赖氨酸多肽模型判定结果,检测半胱氨酸和赖氨酸消耗百分比的均值为30%,结果判定为阳性(消耗百分比的均值>8.32%且>10%),中度反应。
步骤二:开展LuSens试验,检测结果与溶剂对照组相比,诱导倍数小于1,且最大测试浓度细胞活存活率为65%,其余测试浓度细胞存活率均大于70%,结果判定为阴性(与溶剂对照组相比,诱导倍数<1.28,且至少一个测试浓度细胞存活率<70%)。
步骤三:由于上述2个试验结论不一致,开展h-CLAT试验进行确证,检测结果CD86诱导值为200%,CD54诱导值为300%,所有测试浓度细胞存活率均大于80%,结果判定为阳性(CD54诱导值>255%和CD86诱导值>184%,细胞活性≥50%)。
步骤四:综合3选2试验结果,DPRA和h-CLAT结论一致,判定该原料具有皮肤致敏风险。


